La FDA aprueba controversial aerosol nasal para la depresión basado en ketamina
La Administración de Drogas y Alimentos de los Estados Unidos (FDA) aprobó una controvertida droga que ha probado ser efectiva en pacientes con represión resistente a otros medicamentos.
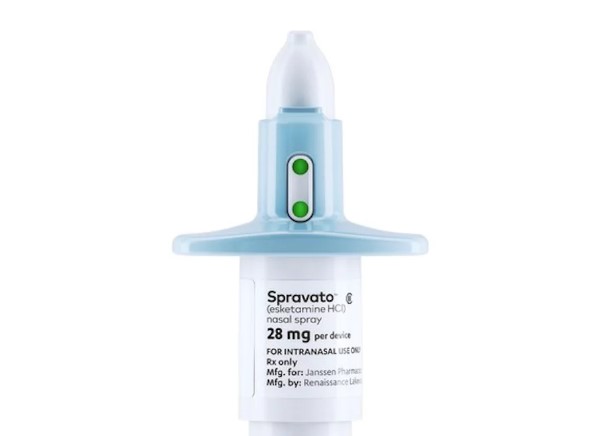
La FDA acaba de aprobar la esketamina para adultos con depresión resistente a tratamientos, en un anuncio histórico que marca el primer nuevo tratamiento de depresión introducido para uso clínico en más de 30 años. El aerosol nasal es un producto químico cercano al polémico anestésico ketamina.
La aprobación del producto, que será comercializado como Spravato, se vio venir el mes pasado después de que un panel asesor de la FDA votó de manera abrumadora a favor de permitir el nuevo tratamiento para uso clínico.
La ketamina ha tenido una historia bastante complicada desde que se desarrolló originalmente en la década de 1960 como un nuevo anestésico. Luego se introdujo rápidamente como una droga contracultural debido a sus curiosas cualidades alucinógenas. Más recientemente, ha sido redescubierto por sus rápidos efectos antidepresivos con las clínicas de ketamina que aparecen en los Estados Unidos y ofrecen dosis a los clientes por miles de dólares.
Polémica aprobación
La luz ver a la comercialización del Spravato no está exenta de controversia. Solo uno de los tres ensayos clínicos a corto plazo que investigaron el fármaco informaron resultados más efectivos que un placebo. Sin embargo, es inusual que un medicamento haya alcanzado la aprobación con una prueba de eficacia tan limitada.
En una declaración de la FDA que acompaña a la aprobación, Tiffany Farchione, directora interina de la División de Productos de Psiquiatría del Centro para la Evaluación e Investigación de Medicamentos de la FDA, señaló: «Hace mucho tiempo que se necesitaban tratamientos adicionales efectivos para la depresión resistente al tratamiento, una condición grave y potencialmente mortal»
«Los ensayos clínicos controlados que estudiaron la seguridad y la eficacia de este medicamento, junto con una revisión cuidadosa a través del proceso de aprobación de medicamentos de la FDA, incluida una discusión sólida con nuestros comités asesores externos, fueron importantes para nuestra decisión de aprobar este tratamiento», concluyó.
El aerosol solamente será aplicado por médicos especializados en consultorios médicos y entornos clínicos controlados. Una vez administrada la dosis recetada, el paciente deberá permanecer dos horas bajo observación y luego podrá irse a casa, pero no podrá llevarse el medicamento.





Compartí tu opinión con toda la comunidad